Von Dr. Heinrich Niehaus, Celle „Das Blaue Jahrbuch“ 1980
Einleitung
Der schöpferische Umgang mit den Erbanlagen, das Spiel mit den Genen, ist auch für interessierte Kaninchenzüchter eine immer wieder faszinierende und nützliche Angelegenheit. Da die Weitergabe der Erbanlagen und damit der Erbinformationen von den Vorfahren auf die Nachkommen nach bestimmten Gesetzmäßigkeiten erfolgt, sind gesteckte Zuchtziele umso schneller und sicherer zu erreichen, je besser der Züchter die Vererbungsvorgänge und ihre Anwendung kennt.
Aus zahlreichen Briefen und Rücksprachen mit Züchtern habe ich den Eindruck, dass das Interesse an Informationen über Vererbungsvorgänge bei Kaninchen eine ansteigende Tendenz aufweist. Das steht zweifellos im Zusammenhang mit einer erhöhten Zuwendung zu den Farbenzwergen und dem dadurch bedingten Bestreben, immer neue Farbenschläge bei den Zwergkaninchen herauszuzüchten. Das gilt auch für den Kurzhaartyp (Rextyp), der bereits mit den meisten Farb- und Zeichnungsmerkmalen der Normalhaarrassen kombiniert worden ist.
Ich möchte mich in diesem Artikel im Wesentlichen darauf beschränken, einfache Körpermerkmale verschiedener Rassen, speziell Fellfarbe und Zeichnung, mit den Erbformeln darzustellen und Beispiele für den Umgang mit diesen Formeln zu geben. Die folgenden Ausführungen sind als Ergänzung zu meinem im Blauen Kaninchen-Jahrbuch 1979 veröffentlichten Beitrag „Einführung in die Vererbungslehre“ (s. Niehaus, 1979) gedacht.
Ich hoffe, im Interesse der Leser zu handeln, wenn ich zum besseren Verständnis der Zusammenhänge auf einige der im erwähnten Artikel bereits behandelten Vorgänge nochmals hinweise. Für diejenigen, die sich eingehender mit den Grundlagen der Vererbung oder speziellen Problemen dieses Fachgebietes befassen möchten, steht eine umfangreiche Literatur zur Verfügung.
Entstehung der Kaninchenrassen
Alle bisher weit über 100 vorhandenen Kaninchenrassen und Farbenschläge stammen vom unscheinbaren grau-braunen europäischen Wildkaninchen (Oryctolagus cuniculus L) ab. Sie sind durch Mutationen und Kombinationen mutierten Erbgutes entstanden.
Mutationen (von mutare, verändern) sind Veränderungen des Erbgutes und der damit verbundenen Erbinformationen. Sie entstehen durch die Kräfte der Natur und werden auf die Nachkommen vererbt. Der Kaninchenzüchter hat keinen Einfluss auf ihre Entstehung. Er kann aber vorhandene Mutationen für züchterische Maß- nahmen nützen. Bei der Entwicklung der verschiedenen Kaninchenrassen haben in erster Linie auffallende Veränderungen der Haarfarbe, das Auftreten von Zeichnungsmerkmalen, der Haarlänge, der Haarstruktur und andere einfache Merkmale eine wichtige Rolle gespielt. Auch Änderungen der Größe, Körperform, Ohren- länge, Ohrenhaltung u. a. sind zur Rassebildung herangezogen worden.
Da letztere nicht durch die Mutation eines einzelnen Genpaares, sondern durch das Zusammenwirken mehrerer, im Einzelnen nicht näher bekannter, meist additiver (summierender) Anlagen zustande kommen, kann auch der Erbgang nicht durch klare Zahlenverhältnisse ausgedrückt werden. Trotzdem ist eine gezielte Beeinflussung dieser Merkmale durch züchterische Maßnahmen möglich. Das gilt ebenso für die Leistungseigenschaften (Fruchtbarkeit, Wachstum, Wolleistung u. a.), auf deren Verbesserung durch züchterische Maßnahmen im Rahmen dieses Artikels nicht näher eingegangen werden kann.
Kombinationen: Man versteht darunter die Vereinigung von zwei oder mehreren unterschiedlichen Erbanlagen, die vor ihrer Kombination getrennt bei verschiedenen Tieren vorhanden waren. Dabei können, wie wir im Folgenden noch an Beispielen erläutern werden, unterschiedliche Farbgene, Farbgene mit Zeichnungsgenen, alle dabei möglichen Kombinationen mit Anlagen für Haarlänge, Haarstruktur u. a. in einem Tier bzw. einem Stamm vereinigt und in reinerbiger Form herausgezüchtet werden. Die bei der Kombination von einfachen Merkmalen vorhandenen Möglichkeiten können hinsichtlich ihrer Zahlenverhältnisse rechnerisch ermittelt werden. Ich werde hierfür einige Beispiele aufzeigen. Es handelt sich bei den errechneten Zahlenverhältnissen allerdings um Wahrscheinlichkeitswerte, die nur im Durchschnitt großer Zahlen ihre Gültigkeit besitzen, bei kleineren Nachkommenzahlen jedoch von den errechneten Werten z. T. erheblich abweichen können.
Die Zahl der Möglichkeiten, unterschiedliche Kombinationstypen zu erzeugen, wird noch dadurch erhöht, dass man die erwähnten Gene und Genkombinationen mit den verschiedenen Größen, Körperformen, Ohrlängen, Ohrhaltung sowie den Leistungseigenschaften kombinieren kann. Dabei ergeben sich praktisch unbegrenzte Kombinationsmöglichkeiten, von denen bisher nur ein relativ kleiner Teil realisiert worden ist. So gesehen sind alle unsere Kaninchenrassen Kombinationstypen, die durch Vereinigung von zwei oder mehr mutierten Genen entstanden sind. Zahlreiche Kombinationen sind zufällig oder unbeabsichtigt bei Kreuzungsexperimenten in Erscheinung getreten. Züchterfleiß und Züchterkönnen haben dazu aber einen wichtigen Beitrag geleistet.
Gensymbole und Erbformeln
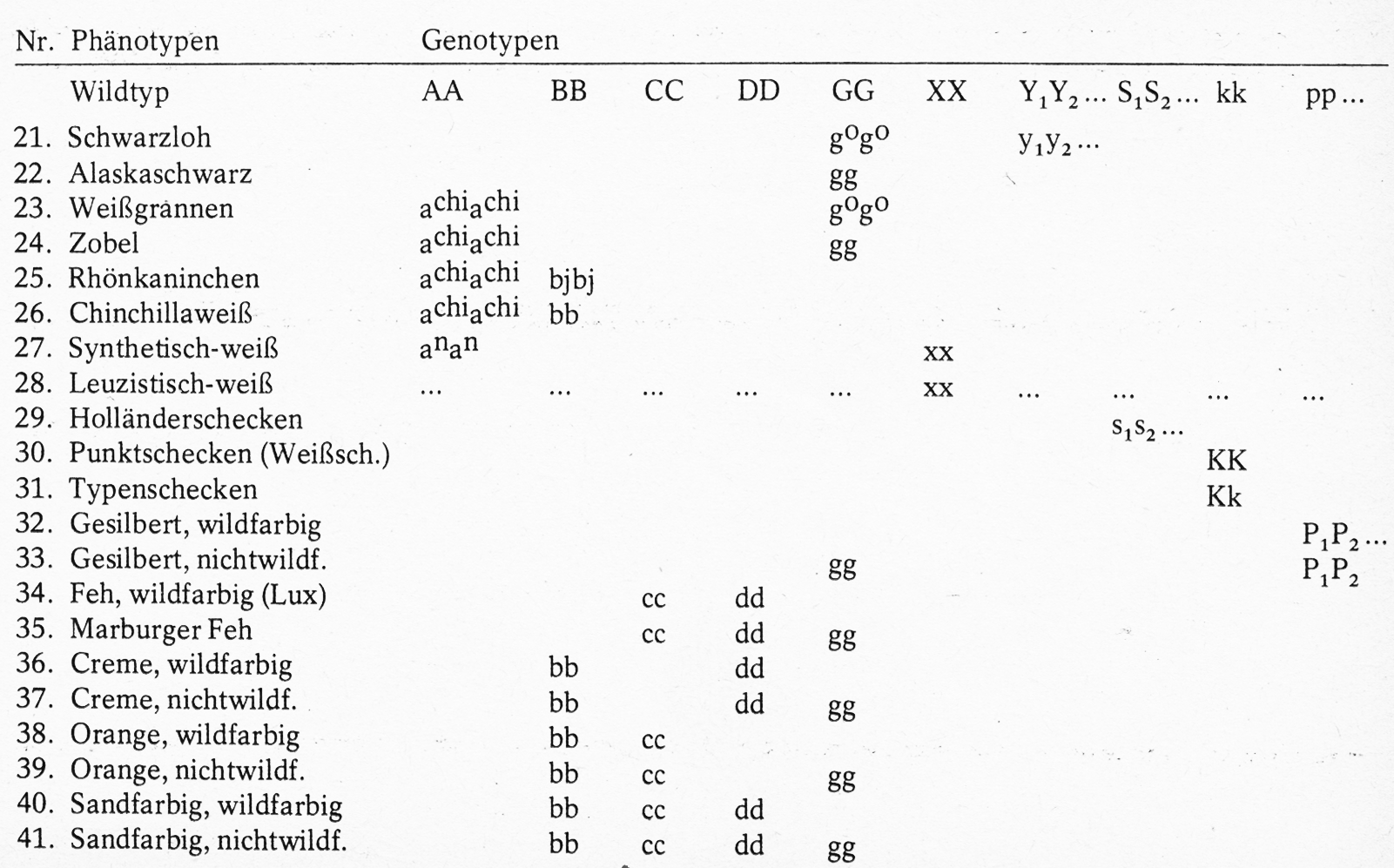
In Tabelle 1 sind die wichtigsten Farb- und Zeichnungstypen der verschiedenen Kaninchenrassen mit ihrem Erscheinungsbild (Phänotypus) und ihrer Erbform (Genotypus) aufgeführt.
Zur Erklärung der Tabelle bedarf es einiger Erläuterungen:
1. Die bekannten Erbanlagen sind- wie das in der Genetik allgemein üblich ist – durch Buchstaben als Gensymbole dargestellt. Die Art der Symbole kann grundsätzlich willkürlich gewählt werden. Die einmal erfolgte Bezeichnung muss dann aber konsequent beibehalten werden, um zu den gleichen Ergebnissen zu kommen. Zum gegenseitigen Verständnis ist es allerdings erforderlich, sich auf eine einheitliche Bezeichnung festzulegen. Ich habe hier die von Prof. Dr. Hans Nachtsheim verwendeten Symbole übernommen (vergl. Nachtsheim und Stengel, 1977). In der englischsprachigen Literatur verwendet man für die gleichen Gene andere Symbole. Wer englische Literatur über Vererbungsvorgänge bei Kaninchen studiert, muss deshalb wissen, welche englischen Symbole den von Nachtsheim verwendeten entsprechen. Vergleiche der Genformeln bei bekannten Genotypen können darüber Aufschluss geben.
2. Alle Chromosomen (Kernschleifen) mit ihren meist zahlreichen Erbanlagen (Gene) sind in den Körperzellen normalerweise paarig vorhanden. Das Kaninchen besitzt 44 = 22 Paar Chromosomen. Davon sind 2 = 1 Paar Geschlechtschromosomen (XX oder XY); alle anderen (42 = 21 Paare) nennt man Autosomen. Die Paarlinge eines Chromosomenpaares heißen homologe Chromosomen, die sich entsprechenden Anlagen Allele oder allele Gene. Will man die Verhältnisse in den Körperzellen darstellen, wie das in Tabelle 1 geschehen ist, so wird das durch Doppelbuchstaben zum Ausdruck gebracht (AA, BB usw.).

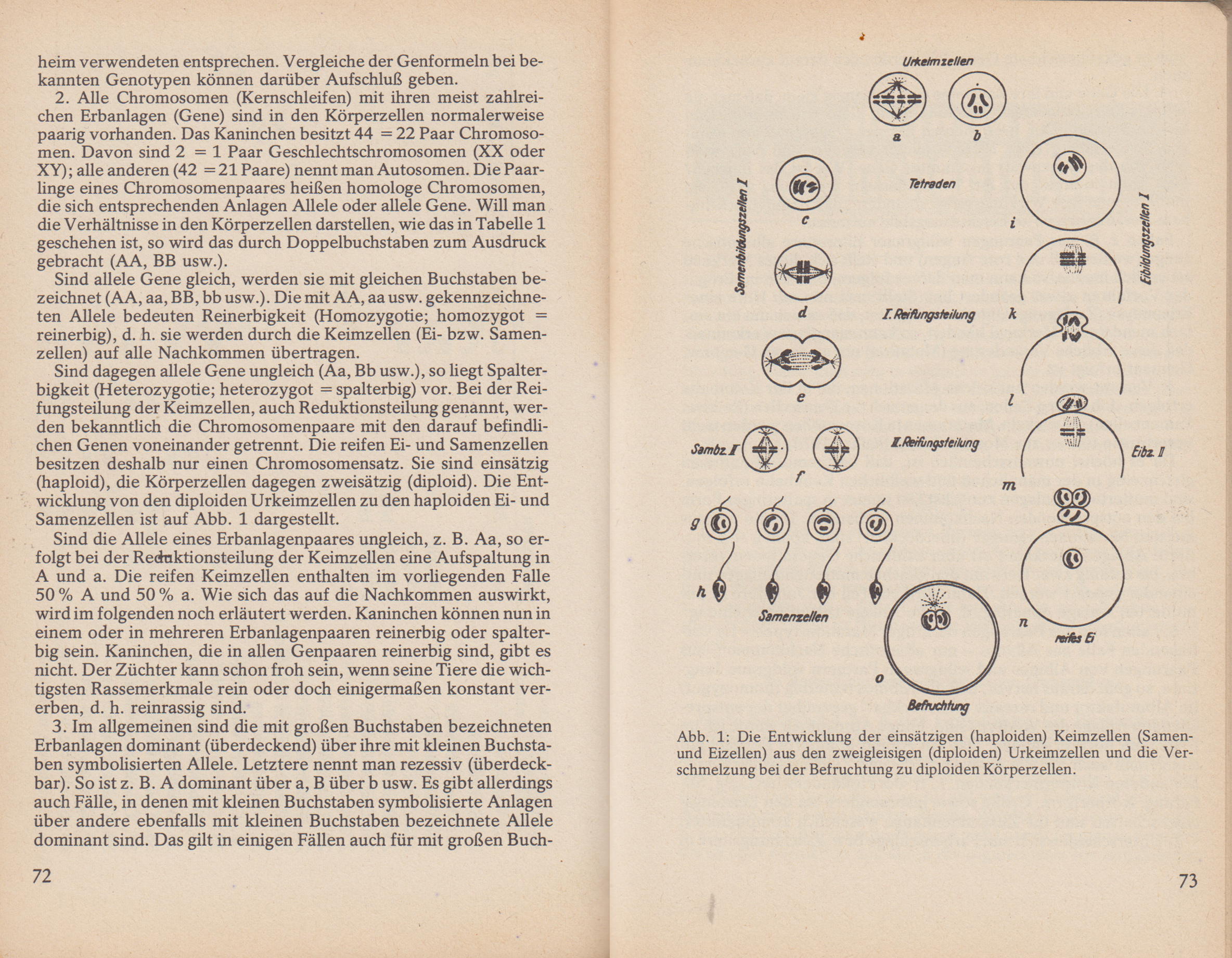
Sind allele Gene gleich, werden sie mit gleichen Buchstaben bezeichnet (AA, aa, BB, bb usw.). Die mit AA, aa usw. gekennzeichneten Allele bedeuten Reinerbigkeit (Homozygotie; homozygot reinerbig), d. h. sie werden durch die Keimzellen (Ei- bzw. Samenzellen) auf alle Nachkommen übertragen. Sind dagegen allele Gene ungleich (Aa, Bb usw.), so liegt Spalterbigkeit (Heterozygotie; heterozygot = spalterbig) vor. Bei der Reifungsteilung der Keimzellen, auch Reduktionsteilung genannt, werden bekanntlich die Chromosomenpaare mit den darauf befindlichen Genen voneinander getrennt. Die reifen Ei- und Samenzellen besitzen deshalb nur einen Chromosomensatz. Sie sind einsätzig (haploid), die Körperzellen dagegen zweisätzig (diploid). Die Entwicklung von den diploiden Urkeimzellen zu den haploiden Ei- und Samenzellen ist auf Abb. 1 dargestellt.
Sind die Allele eines Erbanlagenpaares ungleich, z. B. Aa, so er- folgt bei der Reduktionsteilung der Keimzellen eine Aufspaltung in A und a. Die reifen Keimzellen enthalten im vorliegenden Falle 50% A und 50% a. Wie sich das auf die Nachkommen auswirkt, wird im Folgenden noch erläutert werden. Kaninchen können nun in einem oder in mehreren Erbanlagenpaaren reinerbig oder spalterbig sein. Kaninchen, die in allen Genpaaren reinerbig sind, gibt es nicht. Der Züchter kann schon froh sein, wenn seine Tiere die wichtigsten Rassemerkmale rein oder doch einigermaßen konstant vererben, d. h. reinrassig sind.
3. Im Allgemeinen sind die mit großen Buchstaben bezeichneten Erbanlagen dominant (überdeckend) über ihre mit kleinen Buchstaben symbolisierten Allele. Letztere nennt man rezessiv (überdeckbar). So ist z. B. A dominant über a, B über b usw. Es gibt allerdings auch Fälle, in denen mit kleinen Buchstaben symbolisierte Anlagen über andere ebenfalls mit kleinen Buchstaben bezeichnete Allele dominant sind. Das gilt in einigen Fällen auch für mit großen Buch staben gekennzeichnete Gene. Ich werde noch darauf zurückkommen.
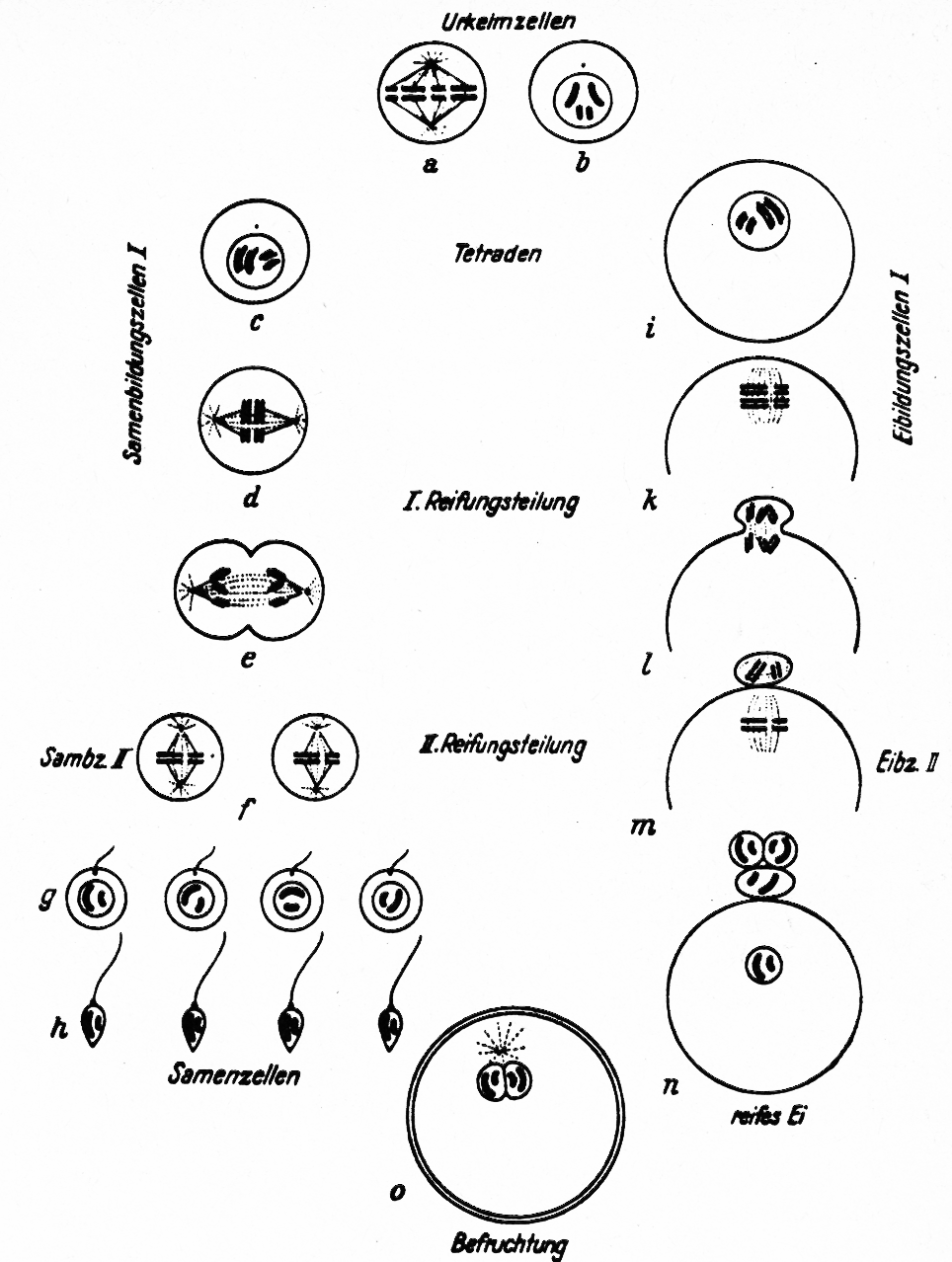
Abb. 1: Die Entwicklung der einsätzigen (haploiden) Keimzellen (Samen- und Eizellen) aus den zweigleisigen (diploiden) Urkeimzellen und die Verschmelzung bei der Befruchtung zu diploiden Körperzellen.
4. Die Gene und ihre Bausteine sind so winzig klein, dass man sie selbst mit millionenfach vergrößernden Elektronenmikroskopen nicht erkennen kann. Kein Mensch hat sie – abgesehen von wenigen Sonderfällen (Heß, 1978) – jemals gesehen, und doch weiß man von der Gegenwart bestimmter Gene. Wie ist das möglich? Man kann indirekt auf ihr Vorhandensein schließen, wenn sie mutieren und ihre Wirkungsweise so ändern, dass dadurch erkennbare Veränderungen im Erscheinungsbild auftreten.
Fallen z. B. aus Paarungen wildgrauer Elterntiere albinotische Junge (weißes Fell und rote Augen) und stellt sich dieses Merkmal als erblich heraus, so kann man daraus folgern, dass sich im Erbgut der Vorfahren etwas geändert hat. Stellt man nun mit Hilfe einer Erbanalyse (Zerlegung, Untersuchung) fest, dass es sich um ein einfach mendelndes Merkmal handelt, so kann man daraus erkennen, dass diese erbliche Veränderung (Mutation) nur an einem Gen bzw. Genpaar erfolgt ist.
5. Vererbt werden nur solche Mutationen, die in der Keimbahn erfolgen, d. h. in den Zellen, aus denen sich die Keimzellen (Ei- bzw. Samenzellen) entwickeln. Mutationen in Körperzellen werden nicht vererbt; sie führen zur Mosaikbildung (Kühn, 1973). Da es höchst unwahrscheinlich ist, dass bestimmte Mutationen gleichzeitig in der männlichen und weiblichen Keimbahn erfolgen, sind mutierte Erbanlagen zunächst fast immer in spalterbiger Form bei den entsprechenden Nachkommen vorhanden.
Da die weitaus meisten Mutationen rezessiv (überdeckbar) sind, können sich mutierte Anlagen unerkannt oft über zahlreiche Generationen vererben, bis zufällig zwei Tiere mit den gleichen mutierten Anlagen miteinander gepaart werden. Dann wird ein Teil der Jungtiere in der mutierten Anlage reinerbig, d. h. die Anlage tritt in Erscheinung.
6. Fallen nun aus Paarungen derartiger Mutationstypen – im vorliegenden Falle aus Albinos – nur albinotische Nachkommen, aus Paarungen von Albinos und wildgrauen Partnern wildgraue Jungtiere, so geht daraus hervor, dass die Albinos reinerbig (homozygot) im Albinofaktor und rezessiv (überdeckbar) gegenüber der entsprechenden Anlage des Wildtyps sind. Einige Ausnahmen werde ich im Folgenden noch erwähnen. Das am Albino erläuterte Beispiel gilt sinngemäß auch für alle anderen Farb- und Zeichnungsmerkmale. Bei anderen Körpermerkmalen, z. B. der Holländerscheckung, Silberung, Körperform, Größe sowie insbesondere bei den Leistungseigenschaften sind die Zusammenhänge wesentlich komplizierter.
7. Unterscheiden sich nun Farbenschläge bzw. Zeichnungstiere in mehr als einem Genpaar vom Wildtyp, so muss das natürlich in der Genformel zum Ausdruck gebracht werden. So hat z. B. das Russenkaninchen mit schwarzen Zeichnungsmerkmalen die verkürzte Genformel anangg, das Marburger Fehkaninchen ccddgg, das sandfarbige Kaninchen (im Standard nicht anerkannt) die Genformel bbccddgg. Dabei muss man in Gedanken immer die nicht angegebenen Allele des Wildtyps hinzufügen. Diese Zusammenhänge dürften besser verständlich werden, wenn wir uns im Folgenden mit der Anwendung der Gensymbole und Genformeln befassen.
Manchmal werden Genformeln auch mit Hilfe eines Bruchstriches angegeben, z. B. ABCDG/AbCDg Dabei werden die von einem Partner stammenden Gene über dem Bruchstrich, die vom andern unter dem Bruchstrich aufgeführt. Bei reinrassigen Tieren kann man sich auch darauf beschränken, die in reinerbiger Form vorhandenen Gene nur einfach aufzuführen, z. B. an Stelle von AAbbCCddgg nur AbCdg zu schreiben. Bei spalterbigen Tieren ist eine derartige Vereinfachung allerdings nicht möglich.
Die Bedeutung der verschiedenen Gensymbole
Nach Nachtsheim ist A der Grundfaktor für Pigmentbildung (Pigment, Farbstoff). Mutiert A zu a und wird es von beiden Eltern auf die Nachkommen übertragen, so wird, unabhängig von den übrigen Erbanlagen, jegliche Pigmentbildung unterbunden. Wir erhalten Vollalbinos (von albus = weiß) mit weißem Haarkleid und roten Augen (Weiße Neuseeländer, Weiße Widder, Hermelin, rotäugig, u. a.). Die rote Augenfarbe entsteht nicht durch Pigmente, sondern durch eine Reflektion des durch die pigmentfreie Iris einfallenden Lichtes von dem mit Blutadern durchzogenen Augenhintergrund. Albinos gibt es im Übrigen auch bei anderen Wild- und Haustieren und auch beim Menschen. In der Wildbahn können sich Albinos immer nur kurzfristig halten. Sie werden im harten Kampf ums Da- sein wegen ihrer auffallenden Fellfarbe und einer verminderten Lebenskraft von Raubtieren, Krankheiten u. a. bald ausgemerzt. Als Haustiere haben sie sich aber unter dem Schutz des Menschen erhalten und sind zu leistungsfähigen Rassen entwickelt worden. Albinotische Menschen sind- wie alle Albinos – besonders empfindlich gegen ultraviolette Strahlen (UV-Strahlen). Zum Schutze ihrer Augen müssen sie dunkle Brillen tragen und die nackte Haut, die kein Pigment bilden kann, gegen Sonnenlicht schützen.
Wie aus Tabelle 1 ersichtlich, gibt es zwischen Vollpigmentiert und Vollalbino mehrere Zwischenstufen, die durch unterschiedliche Veränderungen des Faktors A entstanden und mit einem stufenweisen Abbau des Pigmentes verbunden sind. Man spricht in solchen Fällen von multipler Allelie, durch die im vorliegenden Falle die Albinoserie oder A-Serie entsteht. Ferner kennen wir auch – wie aus Tabelle 1 zu ersehen ist – eine B-Serie und eine G-Serie. Nachstehend ist die A-Serie nochmals im Zusammenhang dargestellt: A-Serie

Man bezeichnet die Typen ad, achi, am und an als Teilalbinos. Gelegentlich werden in der Literatur auch Weiße Wiener und gescheckte Tiere (Holländerschecken, Englische Schecken u. a.) zu den teilalbinotischen Rassen gezählt, weil ihr Haarkleid mehr oder weniger weiß ist. Man sollte m. E. diese irreführende Bezeichnung für die zuletzt genannten Rassen aber nicht verwenden, weil es sich um völlig andere Genotypen handelt als bei den „echten“ Teilalbinos, und weil bei diesen Rassen auch ein weiterer Abbau des Pigmentes niemals zum Vollalbino führt.
In ähnlicher Weise wie A wirkt auch der Faktor X. Bei einer Mutation zu x entstehen ebenfalls Tiere mit weißem Haarkleid. Nur in der Regenbogenhaut (Iris) der Augen wird noch Pigment gebildet. Die Tiere haben blaue Augen (Weiße Wiener, Hermelin, blauäugig, Weiß-Rex, blauäugig, u. a.). Es handelt sich bei blauäugig-weißen Tieren – man nennt sie leuzistisch (von leukos = weiß) – um einen anderen Genotyp als beim Albino. Kreuzungen zwischen beiden Genotypen ergeben pigmentierte Nachkommen (Erklärung s. im Folgenden).
Die Faktoren B, C und D sind die eigentlichen Pigmentfaktoren; G ist ein Farbverteilungsfaktor, der eine zonenweise und ringförmige Aufteilung der Pigmente bewirkt. Diese macht sich besonders bei den wildgrauen Typen bemerkbar. Die schwer definierbare „wildgraue“ Deckfarbe entsteht durch Aufteilung der Pigmente in bläuliche, braune, schwarze und gelbe Zonen. Dunklere oder hellere Decken entstehen durch Unterschiede in der mengenmäßigen Verteilung der Pigmente. Bläst man in das Fell hinein, so bemerkt man einen meist bräunlichen Trichter als Zwischenfarbe. Die Unterfarbe ist blau. Bauchdecke, Innenseite der Läufe, Kinnbackeneinfassung und Unterseite der Blume sind weiß. Wir kennen noch die Schläge Hasengrau, Hasenfarbig, Dunkelgrau und Eisengrau. Die Intensität der Pigmentierung wird durch sog. Modifikationsgene beeinflusst. Darunter versteht man Anlagen, die allein keine Wirkung ausüben, aber die Wirkung anderer Gene (Hauptgene) beeinflussen (vergl. Günther, 1978). Die Bildung des hasengrauen und hasenfarbigen Haarkleides wird durch die sog. Gelbverstärker (y-Faktoren) beeinflusst. Je mehr y-Faktoren vorhanden sind, desto intensiver ist die Ausprägung der Lohe.
Bei blauen, insbesondere bei braunen und gelben Rassen und Farbenschlägen ist die Wirkung des Farbverteilungsfaktors G weniger stark ausgeprägt. Sie kann auch durch züchterische Maßnahmen beeinflusst, z. T. stark zurückgedrängt werden.
Mutiert G zu g, so entfällt die zonenweise Aufteilung des Pigmentes. Die dunkleren Pigmente überdecken dabei die helleren, so dass die Decke einheitlich schwarz, die Unterfarbe bläulich bis blau erscheint. Der Farbfaktor B kann, wie Tabelle 1 zeigt, sowohl zu dem über B semidominanten (teildominanten) Allel Be als auch zu den Allelen bj und b mutieren. Wir haben hier einen Fall, in dem das mit dem großen Buchstaben Be gekennzeichnete Gen über das Allel B dominiert. Im Übrigen entsprechen die Dominanzverhältnisse der Reihenfolge Be, B, bj und b.
Be bewirkt nur in spalterbiger Form (BeB) die als Eisengrau bezeichnete Fellfarbe, die im Standard anerkannt ist. Spalterbig eisengraue Tiere sind bereits wesentlich dunkler als wildgraue. Die Wirkung des Farbverteilungsfaktors G wird weitgehend unterdrückt. Die Decke ist gleichmäßig dunkel; nur die Bauchdeckfarbe ist etwas heller, die Zwischenfarbe nur bräunlich angedeutet. Auch der Nackenteil ist nur andeutungsweise ausgebildet. Reinerbig eisengraue Tiere (BeBe), die zu 25% aus Paarungen der spalterbigen BeB-Eltern fallen, sind schwarz, wenn man von wenigen eisengrauen Haaren absieht. Deren Anzahl kann bei den verschiedenen BeBe-Tieren recht unterschiedlich sein. Die Wirkung des Farbverteilungsfaktors G ist kaum noch oder nicht mehr zu erkennen.
Der Eisengraufaktor kommt in erster Linie bei Riesen- und Widderkaninchen vor, kann natürlich auch auf alle anderen Rassen übertragen werden.
Durch eine Mutation von B in bj entsteht die exotische Japanerzeichnung, bei der die Farben Schwarz und Gelb unregelmäßig über den ganzen Körper verteilt sein sollen, ohne allzu große Farbfelder zu bilden. Besonders bei dieser Rasse zeigt sich, was man durch züchterische Maßnahmen erreichen kann. Dazu gehört die als ideal geltende kreuzweise geteilte Kopf- und Ohrenzeichnung, wobei gelegentlich auch die Farbverteilung auf der einen Körperhälfte umgekehrt sein kann wie auf der anderen. Im Übrigen ist die Variationsbreite bei den Zeichnungsmerkmalen beim Japaner besonders groß. Kein Tier ist genauso wie ein anderes. Krasse Unterschiede von Tier zu Tier sind auch bei Wurfgeschwistern besonders dann zu erwarten, wenn blutfremde Tiere eingepaart wurden. Da die Japanerzeichnung durch ein einfach mendelndes Gen bewirkt wird, sind die z. T. enormen Variationen im Zeichnungsmuster vermutlich weitgehend durch die bereits erwähnten Modifikationsgene bedingt.
Ein weiterer Mutationsschritt von B zu b bewirkt Tiere mit fast ausschließlich gelbem Pigment. Zu den gelben Rassen gehören u. a. Gelbsilber, Gelb-Rexe, Rote Neuseeländer u. a. Die rostrote Fellfarbe der RN wird durch sog. Gelbverstärker (y-Faktoren), die Silberung durch Silberungsfaktoren bewirkt. y-Faktoren spielen auch bei Gelb-Rexen eine zunehmende Rolle. Von den Farbfaktoren bleibt noch der Faktor D, durch dessen Mutation zu d in reinerbiger Form (dd) eine blaue Fellfarbe bewirkt wird (Blaue Wiener, Blau- Rexe u. a.). Es sei noch erwähnt, dass die blaue Fellfarbe nicht durch blaues Pigment, sondern durch eine verdünnte Lagerung der Pigmentkörner zustande kommt. In dem halbdurchsichtigen Medium des Haares wird das einfallende Licht bis auf die Wellenlänge für Blau resorbiert, so dass die Farbe Blau erscheint. Die y-Faktoren, die eine Verstärkung des gelben Pigmentes bewirken, wurden bereits erwähnt. Ihre Wirkung dürfte im Wesentlichen additiv sein, d. h. die Wirkung mehrerer y-Faktoren wird summiert. Sie sind verantwortlich für die rostrote Farbe z. B. bei Roten Neuseeländern, Sachsengold u. a., die Lohfarbe bei Schwarzloh, bei Hasenkaninchen u. a. Je mehr y-Faktoren vorhanden sind, desto intensiver wird die rötliche Fellfarbe. Bei Kreuzungen, z. B. von Roten Neuseeländern mit Tieren, die keine y-Faktoren besitzen, findet eine Verdünnung der y-Faktoren statt. Es tritt ein Verblassen der Lohe in Erscheinung. Die Holländerfaktoren (S₁ S2…) bewirken bekanntlich eine Aufhellung des Haarkleides. Sind nur wenige Holländerfaktoren vorhanden, so macht sich das durch weiße Krallen und/oder weiße Büschel an der Stirn, Nase oder anderen Körperstellen bemerkbar.
Abb. 2: Schematische Darstellung der Holländer-Schecken mit einigen Zwischenstufen von extrem weißen bis zu extrem pigmentierten Typen. Das typische Holländerkaninchen entsteht durch das Zusammenwirken bestimmter Holländerfaktoren.

Bei vermehrter Anwesenheit findet eine Ausdehnung der weißen Flecken statt, die in extremen Fällen über zahlreiche Zwischenstufen bis zu fast weißen Tieren führt (Abb. 2). Eine bestimmte Kombination der Holländerfaktoren führt zu den typischen Ausstellungstieren. Holländerkaninchen können theoretisch reinerbig gezüchtet werden. In der Praxis wird man reinerbige Tiere jedoch kaum erhalten. Mit Hilfe einer geschlossenen Zucht (ohne fremde Blutzufuhr) lässt sich aber mit der Zeit eine einigermaßen konstante Vererbung erreichen. Die Einpaarung blutfremder Tiere kann aber u. U. mühselig erreichte Erfolge mit einem Schlage zunichtemachen, falls man nicht durch Zufall Passertiere erwischt.
Die Punktscheckung (= Engl. Scheckung) wird durch das unvollständig dominante Gen K bewirkt. Zu den Punktscheckenrassen gehören die Englischen Schecken, die Riesenschecken, die gescheckten Widder u. a. In reinerbiger Form (KK) entstehen die sog. Weißlinge, auch Weißschecken oder Chaplins genannt. Letztere werden wegen ihrer schwachen Zeichnung, insbesondere aber auch wegen ihrer verminderten Vitalität als Rasse nicht gezüchtet. Da mit dem Scheckenfaktor K ein Semiletalfaktor (semi = halb; letal = tödlich) gekoppelt ist, erreichen diese Tiere nur selten die Geschlechtsreife. Wesentlich attraktiver und ohne Vitalitätsverluste sind die spalterbigen Typenschecken. Sie gehören mit den Typenmardern zu den Rassen, die nur in spalterbiger Form im Standard anerkannt sind. Rassen mit Englischer Scheckung sind, wie die Holländerkaninchen, nur schwer in der vom Standard verlangten Form zu züchten. Das ist darauf zurückzuführen, dass zwar die Englische Scheckung durch einen einfach mendelnden Faktor (K) bewirkt wird, das Scheckungsmuster aber durch die bereits erwähnten Modifikationsgene erheblich variieren kann, wie jeder Scheckenzüchter zu seinem Leidwesen immer wieder erfahren muss. Durch die Wirkung solcher Modifikationsgene kann man eine ununterbrochene Variationsreihe von fast völlig Weiß bis fast völlig Pigmentiert erreichen. Davon wird teilweise in der Rassezucht auch Gebrauch gemacht. Als extrem heller Typ wird das Hotot-Kaninchen angesehen, wenn auch eine exakte Erbanalyse bei dieser Rasse noch nicht bekannt ist. Einen hohen Pigmentierungsgrad weisen die Widderschecken auf, bei denen die sog. Mantelzeichnung gewünscht wird. Englische Schecken, Deutsche Riesenschecken und Dreifarbenschecken weisen in ihrer Zeichnung keine gravierenden Unterschiede auf, während man bei den Dalmatiner-Schecken eine andere interessante Variation erreicht hat.
Die Silberung gesilberter Rassen (z. B. Helle Großsilber, Deutsche Großsilber, Meißener Widder, verschiedene Farbenschläge der Kleinsilber) wird durch additives Zusammenwirken der dominanten Silberungsfaktoren P1 P2… hervorgerufen. Sie bewirken weiße Spitzen bei einem Teil der Haare. Die Unterfarbe entspricht der der vollpigmentierten Rassen (bläulich bzw. gelblich). Bis zum Haarboden durchgehende weiße Haare – meist als Büschel – sind nicht auf Silberungs-, sondern auf Holländerfaktoren zurückzuführen.
Je mehr Silberungsfaktoren vorhanden sind, desto heller wird die Decke. So besitzen z. B. Helle Großsilber viele Silberungsanlagen, während Deutsche Großsilber und die Kleinsilber über wenige P- Faktoren verfügen. Die Variationsmöglichkeiten sind sehr groß.
Durch züchterische Maßnahmen lassen sich alle Übergänge von extrem hellen zu extrem dunklen Silberungstypen schaffen. Vor Einkreuzungen von gesilberten in einfarbige Rassen ist zu warnen, weil es sehr schwierig und langwierig ist, vorhandene Silberungsfaktoren wieder herauszuzüchten. Das gleiche gilt für die Holländerfaktoren. Durch den Griff zur Pinzette beim Schaufertigmachen von Ausstellungstieren wird das Übel nur vorübergehend vertuscht, aber nicht beseitigt. Gutgläubige Käufer derartiger Tiere sind schon häufig enttäuscht worden.
Die Haarfaktoren (Normalhaar, Langhaar, Kurzhaar, Seiden- haar) sind aus Platzgründen nicht in die Tabelle 1 aufgenommen worden. Da sie bei der Rassebildung jedoch eine nicht unbedeutende Rolle spielen, möchte ich auf ihre Erwähnung nicht verzichten. Wenn man beim Wildtyp die obere Reihe erweitert, ergibt sich folgendes Bild:
Tabelle 2

Zu den Langhaar-Rassen gehören Angora und Fuchskaninchen, zu den Kurzhaar-Rassen die Rexkaninchen mit ihren zahlreichen Farben- und Zeichnungsschlägen. Seit einiger Zeit hat auch das Satinkaninchen (Seidenhaar), bewirkt durch den Faktor sa, ein steigendes Interesse gefunden. Es sei noch erwähnt, dass außer dem Rexfaktor auch noch andere Faktoren, nämlich dek (Deutsch-Kurzhaar) und nok (Normannen-Kurzhaar) eine Verkürzung der Haarlänge bewirken. Da m. W. entsprechende Rassen z. Z. nicht vorhanden sind, möchte ich nicht näher darauf eingehen. – Beim Seidenhaarfaktor handelt es sich um einen Strukturfaktor, der durch Veränderung der Haarstruktur den schönen Seidenglanz des Haarkleides bewirkt.
Im Übrigen kann man die meisten der in Tabelle 1 aufgeführten und die gesondert genannten Haarfaktoren in beliebiger Weise miteinander kombinieren und in reinerbiger Kombination züchten. Eine Ausnahme bilden die Gene der allelen Serien (A-Serie, B-Serie und G-Serie). Die entsprechenden allelen Gene können verständlicherweise zwar in spalterbiger, aber nicht in reinerbiger Form miteinander kombiniert werden. Da sich die Allele jeweils in homologen Chromosomen und dort an der gleichen Stelle befinden, können sich zwar A mit A zu AA, A und a zu Aa, und a mit a zu aa vereinigen; eine Kombination AAaa wäre jedoch nur bei Verdoppelung der Chromosomenzahlen möglich.
Genformeln
Mit Hilfe der in den Tabellen 1 und 2 angegebenen Gensymbole für die verschiedenen Farb- und Zeichnungsmerkmale sowie für Länge und Struktur des Haarkleides sollte es mit einiger Übung und fachlicher Unterstützung gelingen, die Genformeln für alle Rassen und Farbenschläge zu bilden. Größe, Körperform und Leistungsanlagen können dabei nicht berücksichtigt werden, weil man sie nicht exakt durch Symbole zum Ausdruck bringen kann. Auf die Vererbung dieser meist durch additive (summierende) Genwirkung beeinflussten Merkmale und Eigenschaften kann hier nicht näher eingegangen werden. Ich werde mich im Folgenden weitgehend auf die Genformeln für einfache Körpermerkmale beschränken. Zuvor noch ein weiterer Hinweis. Genpaare, die in reinerbiger Form vorhanden sind (AA, aa, BB, bb usw.) werden in der Literatur (Nachts- heim und Stengel, 1977) meist nur einfach (A, a, B, b usw.) aufgeführt, was den Verhältnissen in den einsätzigen Keimzellen (Ei- und Samenzellen) entspricht.
Der Wildtyp wird durch die reduzierte Erbformel ABCDG gekennzeichnet. Die übrigen Gene (X, Y, S usw.), deren Wirkung auch einen Einfluss auf die Fellfarbe des Wildtyps besitzt, werden im Allgemeinen nur dann angegeben, wenn durch ihre Mutation Veränderungen im Erscheinungsbild auftreten. Generell ist es sinnvoll, nur die vom Wildtyp abweichenden Gensymbole in den Erbformeln anzugeben, wie das auch in den Tabellen 1 und 2 geschehen ist. Wenn man so verfährt, d. h. nur vom Wildtyp abweichende Symbole benennt und diese bei Reinerbigkeit der betreffenden Anlage nur einfach darstellt, ergeben sich auf das Wesentliche verkürzte Erbformeln. Nachfolgend einige Beispiele:
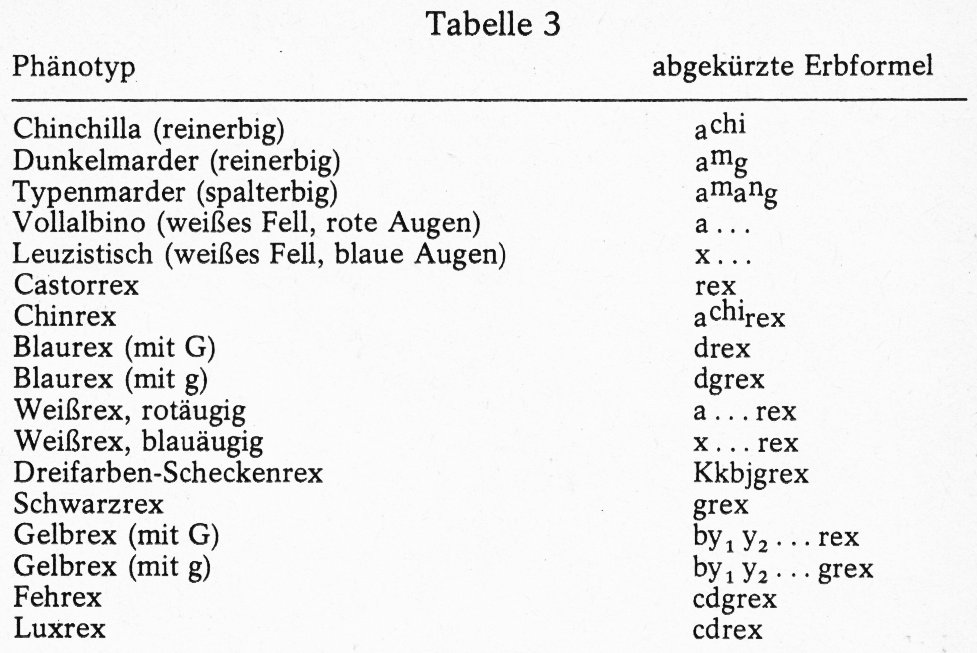
Bemerkungen zu Tabelle 3
1. Bei spalterbigen Tieren (hier Typenmarder) müssen die in spalterbiger Form vorhandenen Anlagen natürlich beide angegeben werden.
2. Die Punkte hinter dem a und x bei albinotischen und leuzistischen Tieren zeigen an, dass hier alle möglichen Farb- und Zeichnungsanlagen vorhanden sein können, deren Wirkung durch den Albinofaktor a bzw. den leuzistischen Faktor x unterdrückt wird. Wir haben z. B. aus Kreuzungen von Weißen Neuseeländern mit Blauen Wienern in der F₁ meist eisengraue und wildgraue, gelegentlich, aber auch schwarze und blaue Jungtiere erhalten. Auch aus Kreuzungen von Angora mit Weißen Wienern fielen in der F₁ ausschließlich pigmentierte Jungtiere. Die meisten zeigten Holländerabzeichen in unterschiedlicher Form. Mehr darüber im Folgenden.
Anleitung zur Verwendung der Genformeln
Will ein Züchter neue Rassen und Farbenschläge herauszüchten, oder scheint es ihm erforderlich, bestimmte Positionen seines Zuchtstammes durch Einkreuzung einer anderen Rasse oder eines anderen Farbenschlages zu verbessern, so kann er sich eine Menge Zeit, Arbeit und Enttäuschungen ersparen, wenn er die Möglichkeiten zunächst auf dem Papier überprüft und erst dann die besten davon in die Praxis umsetzt. Einige im folgenden aufgeführte Beispiele sollen zeigen, wie man dabei verfahren kann.
Ich beginne mit einem einfachen Beispiel, bei dem sich die vorhandene Rasse nur in einem Genpaar vom Wildtyp unterscheidet: Ein Züchter besitzt schwarze Farbenzwerge, bei denen die Fellfarbe zwar den Anforderungen entspricht, Ohren, Körperform und/oder Fell aber noch einer Verbesserung bedürfen. Da der betreffende Stamm bereits weitgehend durchgezüchtet ist, bestehen nur geringe Chancen, die erwähnten Positionen durch weitere Reinpaarungen noch wesentlich zu verbessern. Andere hochwertige Tiere der Farbenschläge stehen dem Züchter nicht zur Verfügung, wohl aber typische wildgraue Farbenzwerge, die in den zu verbessernden Positionen besonders ansprechen. Er möchte nun wissen, wie sich die Fellfarbe bei Einkreuzung der wildgrauen Tiere in der ersten und in den weiteren Generationen vererbt.
Hierüber kann er sich relativ leicht durch ein auf dem Papier vorgenommenes Kreuzungsexperiment informieren.
Schauen wir auf Tabelle 1, Nr. 22, so sehen wir, dass sich die Fellfarbe Alaskaschwarz nur in einem Genpaar vom Wildtyp unterscheidet. Der Farbverteilungsfaktor G des Wildtyps ist zu g mutiert und hat dadurch seine farbverteilende Wirkung eingebüßt, so dass die Fellfarbe schwarz erscheint. Die abgekürzte Genformel für Alaskaschwarz ist demnach gg, für die Allele im Wildtyp GG. Kreuzt man nun wildgraue mit schwarzen Tieren, so ergibt sich folgendes Bild:
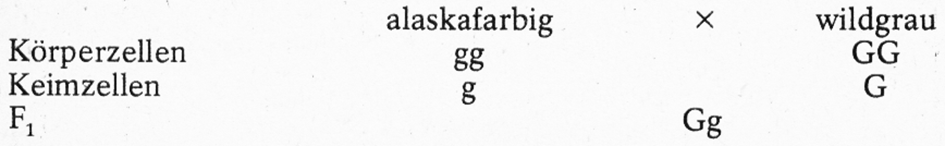
Anmerkung: Wie bereits erwähnt, sind die Chromosomen und die darauf befindlichen allelen Gene in den Körperzellen paarig an- geordnet. Wir bringen das im vorliegenden Falle durch gg bei Alaskaschwarz und GG bei Wildgrau zum Ausdruck. Bei der Reifungsteilung der Keimzellen werden die Paarlinge voneinander getrennt. Alle reifen Keimzellen enthalten bei alaskafarbigen Tieren ein g, bei wildgrauen ein G. Das ist sowohl bei den männlichen Keimzellen (Samenzellen) als auch bei den weiblichen Eizellen der Fall. Es ist deshalb bei den von uns zu behandelnden Beispielen nicht erforderlich, das Geschlecht der Kreuzungspartner anzugeben.
Bei der Befruchtung, bei der die weiblichen Eizellen mit je einer Samenzelle verschmelzen, können in der F₁ (1. Filial-Tochtergeneration) in der Fellfarbe nur einheitliche Jungtiere entstehen (Gg).
Diese sind zu 100% im Erscheinungsbild wildgrau, weil G dominant über g, im Genotyp aber spalterbig ist. Bei Paarungen der spalterbigen F₁-Tiere miteinander tritt eine Aufspaltung in Erscheinung, wie das folgende Beispiel zeigt:
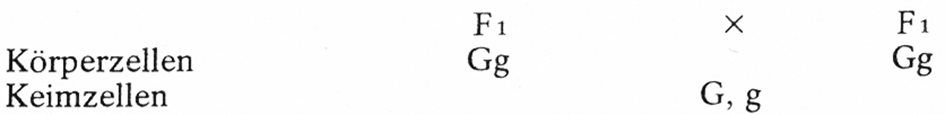
Wir haben nun zwei verschiedene Sorten von Keimzellen, die, weil sie auf beiden Seiten gleich sind, nur einmal aufgeführt werden. Durch das Komma wird angezeigt, dass es sich um unterschiedliche Keimzellen und nicht um spalterbige Körperzellen handelt. Die Möglichkeiten, die sich bei der Befruchtung ergeben (bei der jede Keimzelle des einen Partners mit jeder Keimzelle des anderen verschmelzen kann), können am besten mit Hilfe eines Erbschemas ermittelt werden. Dabei werden die Keimzellen des einen Partners auf der Waagerechten, die des anderen an der Senkrechten eingetragen.
Erbschema 1
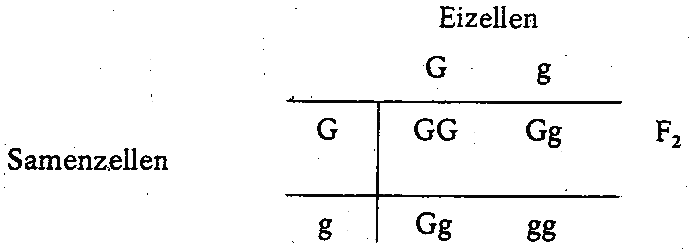
Im vorliegenden Beispiel ergeben sich die Kombinationen GG, Gg, Gg und gg. Da sowohl GG als auch die spalterbige Form Gg eine wildgraue, gg aber eine schwarze Fellfarbe bewirkt, erhält man statistisch, d. h. im Durchschnitt großer Zahlen, ein Verhältnis von Wildgrau Schwarz = 3:1. Zwei der wildgrauen Tiere sind aber : spalterbig (Gg), so dass das Verhältnis von reinerbig Wildgrau spalterbig Wildgrau: reinerbig Schwarz 1:2:1 beträgt.
In sinngemäß gleicher Weise wird verfahren, wenn man blau- wildfarbige, braun-wildfarbige oder gelb-wildfarbige Typen mit wildgrauen kreuzen will. Man muß dabei selbstverständlich auf der einen Seite die Symbole dd für blau-wildfarbig, cc für braun-wild- farbig und bb für gelb-wildfarbig, auf der anderen die entsprechen- den Allele des Wildtyps (DD bzw. CC bzw. BB) verwenden.

Alle Dd-Tiere sind wildgrau, weil sie sich vom Wildtyp nur durch den in spalterbiger Form vorhandenen rezessiven und daher unwirksamen Faktor d unterscheiden.
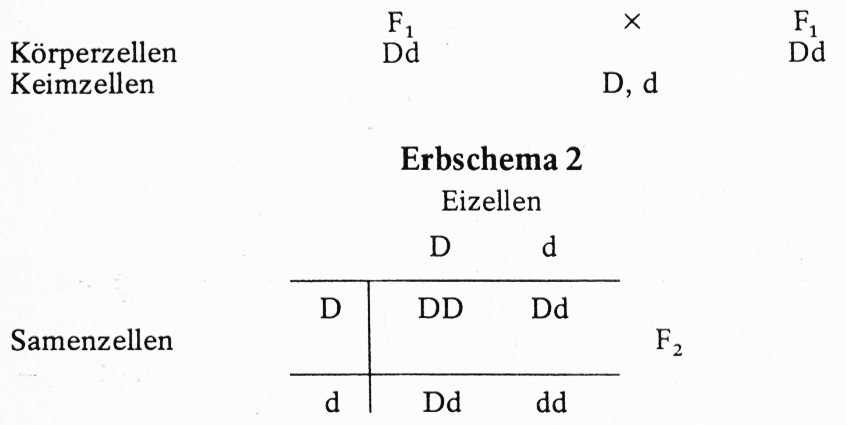
Die Aufspaltungsverhältnisse entsprechen den im Erbschema 1 aufgeführten. Das Verhältnis der Phänotypen Wildgrau : Blauwildfarbig beträgt 3:1, d. h. 75% der Jungtiere sind wildgrau und 25% blauwildfarbig.
Ich hoffe, dass der Leser, am besten in Zusammenarbeit mit anderen interessierten Zuchtfreunden, in der Lage ist, auch andere einfache Kreuzungen auf dem Papier vorzunehmen. Wir kommen nun zum nächsten Schritt, nämlich zu Kreuzungen, bei denen beide Kreuzungspartner in je einem unterschiedlichen Merkmalspaar vom Wildtyp abweichen. Das Ziel dabei ist, die zunächst getrennt bei den Kreuzungspartnern vorhandenen unterschiedlichen Genpaare reinerbig miteinander zu kombinieren und dadurch einen neuen Kombinationstyp zu erhalten. Als Beispiel wollen wir das Weißgrannenkaninchen züchten.
Als Ausgangsrassen dienen Chinchilla (a chiachi) und Schwarzloh (gogo). Bei der Aufstellung der Ausgangsformeln müssen wir uns der im vorhergehenden erwähnten Bemerkung erinnern, dass man den Allelen des einzukreuzenden Tieres immer die entsprechenden Allele des Wildtyps gegenüberstellen muss. In unserem Falle bedeutet das, dass wir dem a chiachi die Allele AA und dem gogo das GG gegenüberstellen müssen. Daraus ergibt sich bei Kreuzungen von Chinchilla x Schwarzloh folgendes Bild:
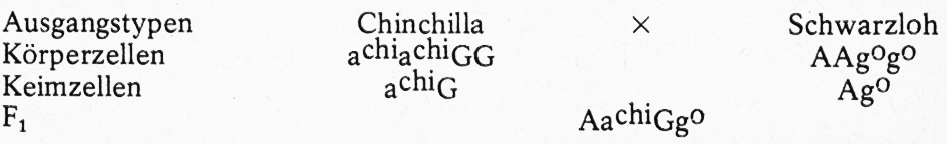
Alle F₁-Tiere sind wildgrau, weil A über achi und G über go dominiert, so dass 100% phänotypisch wildgraue, allerdings doppeltspalterbige F₁-Tiere entstehen. Während es sich nun bei den vorher vorgenommenen Kreuzungen um einen monohybriden (einfach hybriden) Erbgang handelte, ergibt sich hier ein dihybrider (doppelthybrider) Erbgang mit insgesamt 16 Möglichkeiten bei der Befruchtung.
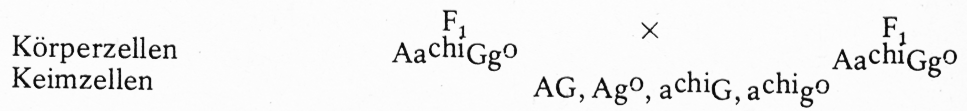
Während die Bildung der Keimzellen bei monohybriden Erbgängen keine Schwierigkeiten bereiten dürfte, sind die Verhältnisse bei dihybriden Erbgängen etwas komplizierter. Ich hoffe aber, dass auch sie nach ein paar aufklärenden Anmerkungen verstanden werden. Bei der Reduktionsteilung findet nicht nur eine Trennung der Chromosomenpaare statt, sondern es erfolgt dabei auch eine beliebige Umschichtung der väterlichen und mütterlichen Chromosomen, so dass Keimzellen mit unterschiedlichem Erbgut entstehen. Diesen Vorgängen muss man auch auf dem Papier Rechnung tragen.
Im vorliegenden Falle können sich 4 unterschiedliche Keimzellensorten, nämlich AG, Ago, achiG und achigo bilden. Andere Kombinationen, z. B. Aachi und/oder Ggo sind nicht möglich, weil es sich ja um Paarlinge handelt, die bei der Reduktionsteilung voneinander getrennt werden.
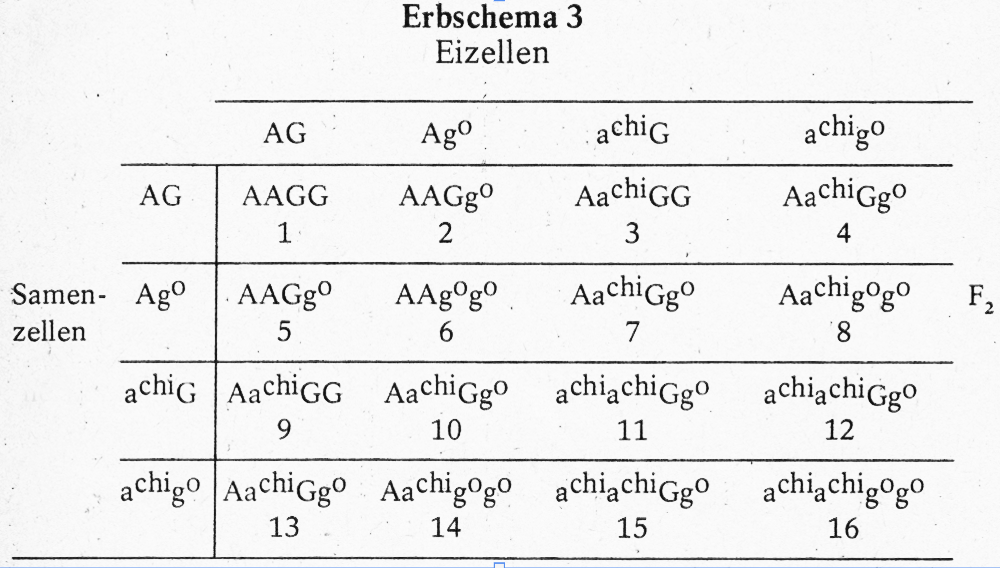
Das phänotypische Verhältnis von Wildgrau : Schwarzloh: Chinchilla : Weißgrannen ist 9:3:3:1.
Von den mit Zahlen bezeichneten Feldern sind 1, 2, 3, 4, 5, 7, 9, 10 und 13 phänotypisch wildgrau. Davon ist der mit 1 bezeichnete Genotyp sowohl in G als auch in A reinerbig (AAGG). Alle anderen wildgrauen Phänotypen sind ein- oder zweifach spalterbig. Der Leser möge sich diese spalterbigen Typen selbst heraussuchen. Die chinchilla- und lohfarbigen Phänotypen sind alle im Chinchillafaktor bzw. im Lohfaktor reinerbig, in dem jeweils anderen Faktor einfach spalterbig. Von den lohfarbigen Tieren ist das Tier 6 in beiden Anlagenpaaren reinerbig, von den chinchillafarbigen liegt Reinerbigkeit bei 11 vor.
Das mit 16 bezeichnete Tier ist ein völlig neuer Kombinationstyp (achiachigogo), der bei 1 von 16 Jungtieren zu erwarten ist. bei diesem „Chinchilla-Loh“ wird die Ausbildung des beim Loh vorhandenen gelben Pigments durch den Chinchillafaktor verhindert, so dass die gelben bzw. roten Zeichnungsmerkmale und Spürhaare des Lohkaninchens pigmentlos weiß sind.
Noch ein Hinweis: Wenn man das Erbschema richtig aufgestellt hat, befinden sich die reinerbigen Typen in der Diagonalen, in diesem Falle 1, 6, 11 und 16.
Bei unseren bisherigen Beispielen sind wir immer von Tieren ausgegangen, bei denen die verwendeten Erbanlagen in reinerbiger Form vorhanden waren. Nun ist es nicht selten so, dass ein oder beide Ausgangstiere spalterbig sind. Das muss natürlich bei der Aufstellung der Erbformeln berücksichtigt werden. Ich möchte das an einem Beispiel zeigen.
Werden die aus der erwähnten Kreuzung Chinchilla X Schwarzloh erhaltenen F₁-Tiere auf reine Schwarzloh zurückgepaart, so ergibt sich folgendes Bild:
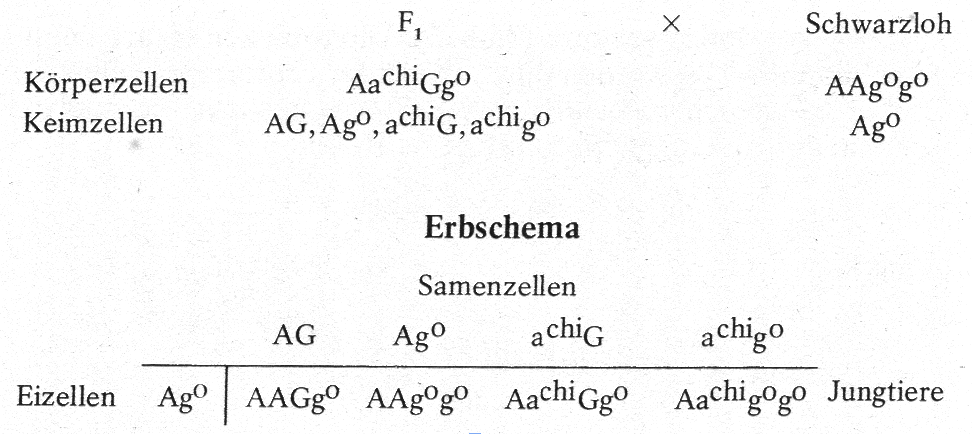
Bei der Rückpaarung fallen 50% wildgraue und 50% lohfarbige Jungtiere. Von den wildgrauen Tieren ist die Hälfte einfach-, die andere Hälfte zweifachspalterbig. Die lohfarbigen Jungtiere sind zu 100% reinerbig im Lohfaktor, 50% davon besitzen eine andere Anlage (Aachi) in spalterbiger Form. Werden solche, äußerlich nicht erkennbaren Tiere durch Zufall miteinander gepaart, so sind u. a. 25% Weißgrannen zu erwarten. Bei Rückpaarung der F₁ mit Chinchilla ergeben sich analoge Verhältnisse. Der Leser möge versuchen, die Rückpaarung mit Chinchilla auf dem Papier vorzunehmen.
Ich möchte zum Abschluss noch auf zwei interessante Erbgänge hinweisen, aus denen die in Celle von mir gezüchteten Schwarzgrannen und Celler Weiße bzw. das blauäugige Angorakaninchen hervorgegangen sind.
Die Züchtung des Schwarzgrannenkaninchens ist u. a. im Blauen Kaninchen-Jahrbuch 1969 ausführlich beschrieben (Niehaus, 1969). Über die Züchtung des blauäugigen Angorakaninchens ist mehrfach berichtet worden (Niehaus, 1954, 1956 und 1957). Beim Schwarzgrannenkaninchen und Celler Weißen ist besonders interessant, dass Tiere mit weißem Fell und braunen Augen aus zwei pigmentierten Rassen, nämlich aus Roten Neuseeländern (Abb. 3) und Chinchilla (Abb. 4) entstehen konnten.
Erbgang

Alle F1-Tiere sind hasengrau (Abb. 5). Die rötlichen Haare beim sonst wildgrauen Typ werden durch die in der Erbformel nicht aufgeführten, zusätzlich vorhandenen y-Faktoren bewirkt. Sie spielen bei dem angestrebten Endprodukt keine Rolle:

Abb. 3: Eine der für die Neuzüchtung der Schwarzgrannen bzw. Celler Weißen verwendete Rote-Neuseeländer-Häsin.

Abb. 4: Für die unter 3 genannte Neuzüchtung u. a. verwendeter Chinchillarammler.

Dabei sind in der verkürzten Erbformel die y-Faktoren nicht angegeben. Ferner besitzen alle Tiere den Farbverteilungsfaktor G.
Fasst man die im Schema angegebenen Typen nach ihrer Erscheinungsform zusammen, so ergeben sich
9 hasenfarbige
3 chinchillafarbige
3 rötlichgelbe Tiere und
1 Tier mit weißer Fellfarbe.
Die weiße Fellfarbe ist dadurch zu erklären, dass die Ausbildung des gelben bzw. rostroten Pigments der Roten Neuseeländer durch den Chinchillafaktor verhindert wird, andererseits aber der Faktor für gelbes Pigment der Roten Neuseeländer die Ausbildung aller anderen Pigmente, bis auf das der Iris und der unerwartet aufgetretenen dunklen Grannenspitzen unterbindet. Letztere haben zu dem Namen „Schwarzgrannenkaninchen“ geführt. Die Ursache für die Pigmentbildung in der Regenbogenhaut und einigen Grannenspitzen ist noch ungeklärt. Später ist es uns dann gelungen, durch fortlaufende Selektion die Anzahl der pigmentierten Grannen mehr und mehr zurückzudrängen und schließlich Tiere mit reinweißem Fell und dunkelbraunen Augen zu erhalten. Die in Abb. 6 gezeigten Jungtiere besitzen bereits ein fast reinweißes Haarkleid. Die reinweißen Tiere wurden später „Celler Weiße“ genannt. Sie zeichneten sich durch besondere Vitalität und Fruchtbarkeit aus. Unser Vorhaben, diesen Typ langhaarig zu züchten, konnte wegen der Übernahme anderer Aufgaben leider nicht mehr realisiert werden.
Bereits einige Jahre vorher hatten wir das blauäugige Angorakaninchen gezüchtet, das durch eine reinerbige Kombination des Langhaarfaktors v mit dem Faktor für Leuzismus x entstanden ist und die abgekürzte Genformel vvxx aufweist.

Alle F₁-Tiere sind normalhaarig und pigmentiert. Es handelt sich hierbei also um eine Kreuzung, bei der aus reinerbig-weißen Ausgangsrassen (Angora und Weiße Wiener) in der F₁ pigmentierte Jungtiere in Erscheinung treten. Diese für den Nichtfachmann erstaunliche Erscheinung ist genetisch aus der Formel AaXxVv leicht zu erklären. Da A über a und X über x dominieren, können a und x, die in reinerbiger Form eine Pigmentierung verhindern, in spalterbiger Form nicht mehr wirksam werden, so dass Jungtiere mit pigmentiertem Haarkleid auftreten. Die Art der Pigmentierung und das Auftreten von Zeichnungsmerkmalen sind von den jeweils bei den genannten weißen Rassen vorhandenen Farb- und Zeichnungsgenen abhängig. Da die bei den weißen Tieren vorhandenen Farb- und Zeichnungsgene nicht bekannt sind, können die F₁-Tiere alle möglichen Farb- und Zeichnungsmerkmale zeigen.
Wir erhielten bei unseren Paarungen in der F₁ in erster Linie eisengraue, wildgraue und schwarze Tiere, die mehr oder weniger mit Holländerabzeichen behaftet waren (Abb. 7). Bei der Weiterzüchtung fielen außerdem auch blaue, braune und gelbe Jungtiere, teils mit, teils ohne Holländerabzeichen. Die Holländerfaktoren stammten bei unseren Paarungen ausschließlich von den Weißen Wienern, da bei Kreuzungen von Angora mit vollpigmentierten Rassen nur vollpigmentierte Jungtiere erhalten wurden.
Bei dieser Gelegenheit sei noch auf einen besonderen albinotischen Genotyp (aaxx) hingewiesen, der bei Paarungen mit albinotischen Partnern ausschließlich albinotische Jungtiere und bei Paarungen mit leuzistischen (blauäugigen) Partnern ausschließlich blauäugig weiße Jungtiere ergibt.
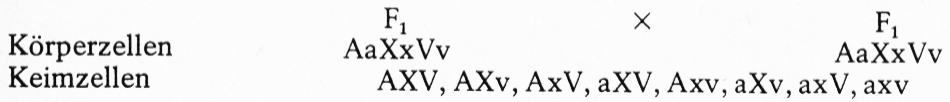
Auf eine Darstellung des Erbschemas muss aus Platzgründen verzichtet werden, da es sich um einen trihybriden (dreifachhybriden) Erbgang mit 8×8 = 64 Kombinationsmöglichkeiten in der F2 handelt. Dem interessierten Leser dürfte es aber nicht schwerfallen, dies in der bei mono- und dihybriden Erbgängen demonstrierten Weise nachzuvollziehen.
Ich möchte mich auf einige Bemerkungen zum Ergebnis beschränken. Da von den 64 Kombinationsmöglichkeiten einige mehrmals vorkommen und unterschiedliche Genotypen z. T. gleiche Phänotypen bewirken, erhalten wir von den 64 Kombinationsmöglichkeiten nur 27 genotypisch unterschiedliche Formen und 6 verschiedene Phänotypen, nämlich:
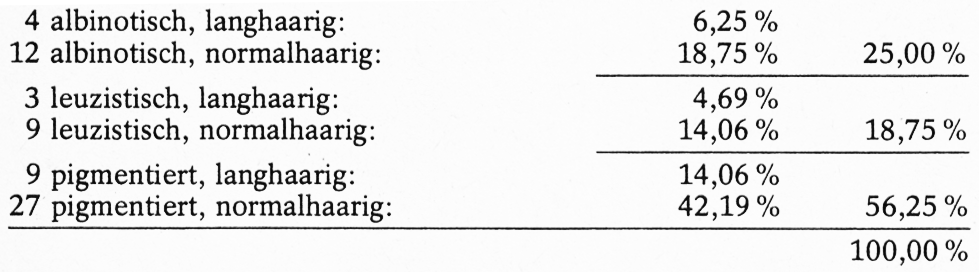
Damit möchte ich dieses Kapitel abschließen. Selbstverständlich lassen sich nach dem gleichen Schema auch mehr als dreifachhybride Erbgänge rechnerisch durchführen. Die dabei auftretenden Kombinationsmöglichkeiten werden aber so zahlreich, dass hier auf eine Darstellung verzichtet werden muss.
Abschließende Bemerkungen
Ich habe mich bemüht, in den vorstehenden Ausführungen genetisch interessierten Kaninchenzüchtern die Grundlagen für die Entstehung der Erbformeln zu erklären, die genetischen Grundtypen in Tabelle 1 zusammenzustellen und den Umgang mit den Erbformeln an Beispielen zu erläutern. Im Rahmen dieses begrenzten Artikels mussten natürlich viele interessante Fakten unerwähnt bleiben, andere konnten nicht mit der wünschenswerten Ausführlichkeit behandelt werden. Ich hoffe aber, durch diesen und den im Blauen Kaninchen-Jahrbuch 1979 erschienenen Artikel das bereits vorhandene Interesse an Vererbungsvorgängen und ihre Beeinflussung auf die Züchtung weiter geweckt zu haben. Vorhandene Unklarheiten können am besten in Gemeinschaftsarbeit unter Anleitung eines mit der Vererbung vertrauten Züchters beseitigt werden. Je besser man die Zusammenhänge kennt, desto interessanter und erfolgreicher kann das eingangs erwähnte Spiel mit den Genen gestaltet werden.
Abb. 5: Hasengraue F₁-Jungtiere aus einer Kreuzungspaarung von Roten Neuseeländern mit Chinchilla. Die Tiere zeichneten sich durch eine besonders große Vitalität aus.


Abb. 6: Celler Weiße, die bereits weitgehend dem Zuchtziel entsprechen.
Abb. 7: F₁-Jungtiere mit ihrer Mutter (Weiße Wiener) aus einer Kreuzung von Angora mit Weißen Wienern. Man beachte die Holländerzeichnung.

Literaturverzeichnis
Niehaus, H.: Einführung in der Vererbungslehre, Das Blaue Kaninchen-Jahrbuch 1979, Verlag Oertel + Spörer, Reutlingen, 1978
Nachtsheim, H.: Vom Wildtier zum Haustier, Zweite Auflage, Verlag Paul Parey, Berlin und Hamburg, 1949
Kühn, A.: Grundriss der Vererbung, S. 118, Quelle & Meyer, 1973
Nachtsheim, H., und Stengel, H.: Vom Wildtier zum Haustier, Dritte Auflage, Verlag Paul Parey, Berlin und Hamburg, 1977
Günther, E.: Grundriss der Genetik, VEB Gustav Fischer Verlag, Jena, 1978
Angermann, K., in: Grzimeks Tierleben, Bd. XII, Säugetiere 3, Kindler Verlag AG, Zürich, 1972
Niehaus, H.: Züchtung des Schwarzgrannenkaninchens, Blaues Kaninchen- Jahrbuch 1969, Oertel + Spörer, Reutlingen 1968
Niehaus, H.: Neuzüchtung eines leuzistischen (blauäugigen) Angorakaninchens. Dt. Kleintierzüchter, Ausg. Kaninchen, (24), 1954. Ferner in „Kleintierzucht in Forschung und Lehre, Celler Jahrbuch“, 1954, Oertel + Spörer, Reutlingen 1955
Niehaus, H.: Die Weiterzüchtung des leuzistischen (blauäugigen) Angorakaninchens in „Das Blaue Kaninchen-Jahrbuch 1957“, Oertel + Spörer, Reutlingen 1956. Ferner in: Kleintierzucht in Forschung und Lehre, Celler Jahrbuch 1956, Oertel + Spörer, Reutlingen 1957.
Heß, D.: Genetik, Grundlagen – Erkenntnisse, Entwicklungen der modernen Vererbungsforschung. Verlag Herder, Freiburg 1972.